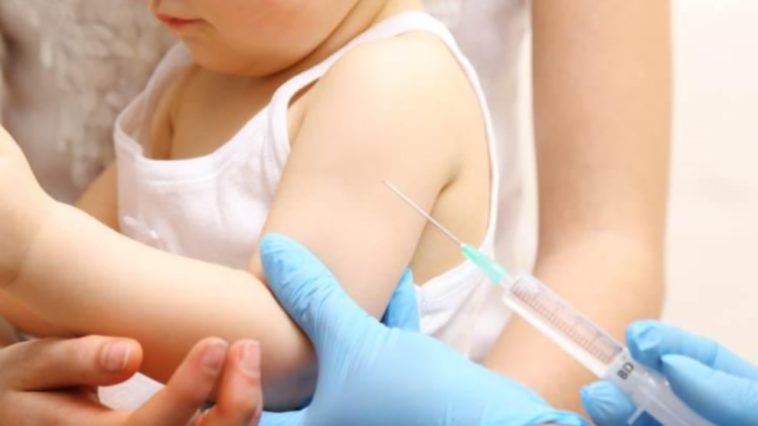
Este martes, la farmacéutica Moderna informó que comenzó en Estados Unidos los ensayos clínicos de su vacuna contra la COVID-19 en niños de entre 6 meses y 12 años.
El director ejecutivo de la empresa, Stephane Bancel, señaló en un comunicado, “estamos felices de empezar este estudio en fase 2/3 de mRNA-1273 en niños sanos en Estados Unidos y Canadá“.
Moderna, detalló que los ensayos en 6 mil 750 menores, lo que les ayudará a evaluar la posible seguridad e inmunogenicidad de la vacuna en la población de menor edad.
Por su parte, las autoridades sanitarias de Estados Unidos, afirmaron que el número de niños que han enfermado por COVID-19 es menor que el de los adultos, pero pueden infectarse y propagar el virus.
De acuerdo con Moderna, el estudio se realizará en dos partes, en la Parte 1, cada participante de dos años a menos de 12 años puede recibir uno de dos niveles de dosis (50 ug o 100 ug).
Los participantes de de seis meses a menos de 2 años recibieran uno de los tres niveles de dosis (25 ug, 50 ug y 100 ug).
Luego se llevará a cabo un análisis intermedio para determinar qué dosis se utilizará en la Parte 2, que será la parte del estudio de expansión controlada con placebo.
La vacuna Moderna contra la COVID-19 está autorizada para su uso bajo una autorización de uso de emergencia en mayores de 18 años.
https://twitter.com/moderna_tx/status/1371779513865154562