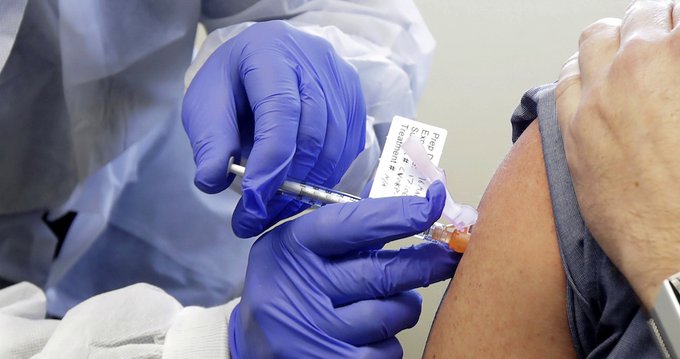
Este viernes la farmacéutica estadounidense Pfizer presentó una solicitud a los reguladores de salud de Estados Unidos para que le autoricen el uso de emergencia de su vacuna contra el Covid-19.
En un comunicado Pfizer dio a conocer que la aprobación de la vacuna que desarrolla con su socio aleman BioNTech sería un paso crucial para ofrecer una inmunización extendida que ayude a detener la pandemia.
Durante la semana Pfizer y BioNtech, reportaron que los resultados finales de su ensayo arrojaron un porcentaje de efectividad del 95 %.
La firma espera que la FDA apruebe la autorización de uso de emergencia para mediados de diciembre, lo cual podría empezar a enviar dosis de forma casi inmediata.
Pfizer indicó que espera tener 50 millones de dosis de vacunas lista este año, suficientes para proteger a 25 millones de personas.
De acuerdo con una uente conocedora del proceso a Reuters un comité asesor de la FDA planea reunirse de forma tentativa entre el 8 y el 10 de diciembre para hablar sobre la vacuna.